難病治療薬タブネオスで20人死亡?肝機能障害や国内外の動向を詳しく解説
全身の血管に炎症が起きる難病、ANCA関連血管炎の治療薬として期待されていた「タブネオス(一般名:アバコパン)」について、衝撃的なニュースが飛び込んできました。日本国内でこの薬を使用していた患者さんのうち、20人が死亡したという報告があったのです。
この記事では、製薬会社であるキッセイ薬品工業が発表した資料や、インタビューフォームに基づき、何が起きているのか、どのようなリスクがあるのかを解説します。
1. タブネオスを巡る現状:20人の死亡報告と製薬会社の対応
2026年5月、タブネオスの製造販売元であるキッセイ薬品工業は「タブネオスの適正使用について」という重要な文書を公表しました。
報道によると、2022年の発売開始からこれまでに国内で約8,500人の患者に使用されましたが、その中で20人の死亡例が報告されたとのことです。特に注目されているのは、その死因や副作用の内容です。死亡した20人のうち、13人が「胆管消失症候群(たんかんしょうしつしょうこうぐん)」という重い肝機能障害を発症していたとされています。
製薬会社による現在の勧告
この事態を受け、会社側は直ちに販売中止や回収を行うのではなく、以下の「慎重な運用」を医療機関に求めています。
1. 新規患者への使用を当面控えること
2. 継続中の患者には、リスクと代替治療を説明した上で、投与を続けるか慎重に判断すること
これは「薬が直ちにダメだ」と断定されたわけではありませんが、「安全性が十分に確認できるまで、新しく使い始めるのはストップしましょう」という極めて警戒度の高い通達です。
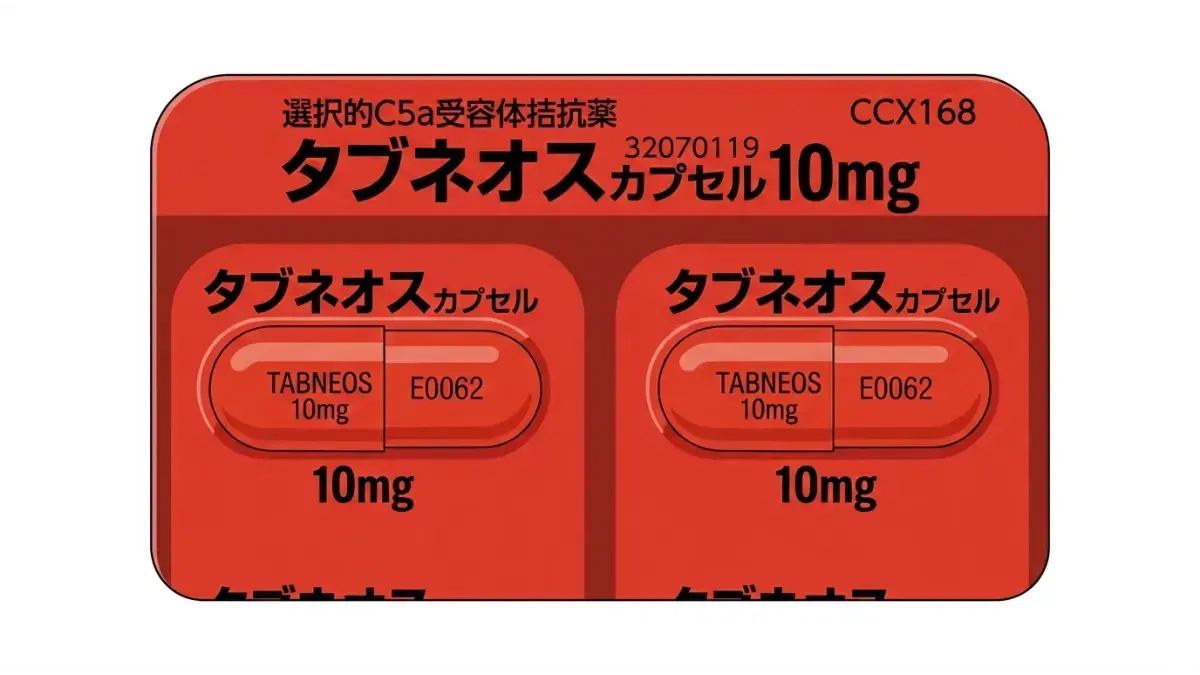
2. そもそも「タブネオス」とはどんな薬か?
タブネオス(アバコパン)は、「顕微鏡的多発血管炎(MPA)」や「多発血管炎性肉芽腫症(GPA)」といった、難病に指定されている血管炎の治療薬です。
私たちの体には、細菌などから守る「補体(ほたい)」という仕組みがあります。しかし、この病気では補体の一部である「C5a」という物質が暴走し、自分自身の血管を攻撃して激しい炎症を引き起こします。
タブネオスはこの「C5a」の働きをピンポイントでブロックする、世界初の「選択的C5a受容体拮抗薬」として登場しました。これまでの治療では強力なステロイド薬を大量に使う必要があり、その副作用が大きな課題でした。タブネオスはステロイドの使用量を減らしつつ、病気を抑える「画期的な新薬」として期待されていたのです。
3. 海外(アメリカ・欧州)で起きている深刻な疑義
今回の日本国内での死亡報告の背景には、実は海外での「承認取り消し」に向けた動きも深く関係しています。キッセイ薬品の資料によると、欧米ではさらに厳しい状況に陥っています。
米国(FDA)の動き
2026年3月、アメリカの食品医薬品局(FDA)は、タブネオスを服用した患者に「重度の薬物誘発性肝障害」が発生したとして注意喚起を行いました。
さらに衝撃的なのは、2026年4月です。FDAは、「承認申請書類に重要な事実に反した記載が含まれていた」「新たに得られた情報では有効性が示されていない」として、米国における承認の撤回(取り消し)を提案しました。
欧州(EMA)の動き
欧州医薬品庁(EMA)でも、国際共同治験データの整合性に疑義が生じたとして、現在レビューが行われています。
つまり、薬の副作用という安全面の問題だけでなく、「そもそもこの薬は本当に効くのか?」「承認時のデータは正しかったのか?」という、薬としての根幹が揺らぐ事態になっているのです。
4. 肝機能障害と「胆管消失症候群」について
今回の報告で最も恐れられている副作用が肝機能障害です。特に死亡例の多くに見られた「胆管消失症候群」について詳しく解説します。
肝機能障害とは
肝臓は「体の化学工場」と呼ばれ、毒素を分解したり、消化を助ける「胆汁(たんじゅう)」を作ったりしています。薬の影響で肝臓の細胞が壊れると、これらの機能がストップし、全身に毒素が回ったり、黄疸(おうだん)が出たりします。
胆管消失症候群(VBDS)とは
胆管とは、肝臓で作られた胆汁を十二指腸まで運ぶ「管」のことです。胆管消失症候群とは、何らかの原因(この場合は薬の副作用)によって、肝臓の中の細い胆管が壊れて失われてしまう極めて珍しい疾患です。
胆汁が流れなくなると肝臓の中に溜まり、肝細胞を破壊し、最終的には肝不全に至ります。一度失われた胆管は再生が難しく、命に関わる非常に重篤な状態となります。

5. インタビューフォームから見る「副作用の頻度」
「医薬品インタビューフォーム(IF)」には、承認前に行われた臨床試験の結果が詳細に記されています。これを見ると、肝機能障害のリスクは以前から認識されていたことがわかります。
臨床試験での肝障害の頻度
第III相臨床試験(ADVOCATE試験)におけるデータは以下の通りです。
– 肝機能障害に関連する副作用の発生率
– タブネオス群:13.3%(166例中22例)
– 比較対象(プレドニゾン群):11.6%(164例中19例)
– そのうち「重篤」と判定されたもの
– タブネオス群:5.4%(9例)
– 比較対象(プレドニゾン群):3.7%(6例)
この時点でも、従来の治療法(ステロイド治療)より肝障害のリスクがわずかに高い傾向にありました。また、市販後の全例調査でも、重大な副作用として「肝機能障害」が一番上に挙げられており、肝細胞損傷や胆汁うっ滞性肝炎が報告されていました。
しかし、当時は「適切な管理をすれば使用可能」と判断されていましたが、市販後に想定を上回るペースで重症化・死亡例が出てしまったことが、今回の事態を深刻化させています。
6. 患者さんとご家族が今すべきこと
この記事を読んで不安になった方も多いと思いますが、治療を行っている処方医にとっても同様です。製薬メーカーが「適正使用」に関する情報を開示すると、医師は開示された情報をもとに治療方針を再検討するケースがあります。まずは主治医へ継続の可否や、治療状況、肝機能について再度相談しましょう。
相談の目安となる症状
もしタブネオスを服用中で、以下のような症状が出た場合は、すぐに主治医に連絡してください。これらは肝機能障害のサインである可能性があります。
– 白目が黄色くなる、肌が黄色っぽくなる(黄疸)
– 尿の色が濃い茶色になる(紅茶のような色)
– 激しい倦怠感(体がだるい)、食欲不振
– 吐き気、嘔吐
– お腹の右上あたりの痛み
7. まとめ
今回のタブネオスを巡る騒動は、難病治療の現場に大きな波紋を広げています。ポイントをまとめると以下の通りです。
– 国内で8,500人中20人の死亡が報告され、その多くが肝臓の「胆管消失症候群」を伴っていた。
– 米国では「データの信憑性」や「有効性の欠如」を理由に承認取り消しの提案が出されている。
– 日本では現在、承認は継続しているが「新規の使用は控える」よう強い注意喚起が出ている。
– 臨床試験時から肝障害のリスクは指摘されていたが、市販後にその重症度が浮き彫りになった。
新薬は、これまでの薬で救えなかった人を救う希望である一方、数千人規模で使われて初めて判明する未知のリスクを孕んでいます。今回の事態は、まさにその「市販後の安全性」の難しさを示しています。
まずは、患者さんの安全が最優先です。もし不安がある場合は、キッセイ薬品工業が設置している「タブネオス専用ダイヤル」や、各病院の相談窓口を活用し、正しい情報を得るようにしてください。