トラゼンタ後発品参入に追い風!「用法・用量特許」の無効判決を巡る最新動向
2型糖尿病治療薬として広く処方されているDPP-4阻害剤「トラゼンタ(一般名:リナグリプチン)」。そのジェネリック医薬品(後発品)参入を巡る争いで、大きな進展がありました。
2026年12月の参入を目指す後発品メーカー各社にとって、最大の障壁の一つとされていた「用法・用量特許」に対し、知的財産高等裁判所(知財高裁)が「特許は無効」とする審決を維持する判決を下したのです。
1. 争点となった「用法・用量特許」とは?
トラゼンタの標準的な使い方は「1日1回5mgを服用する」というものです。実は、この当たり前のような服用ルールそのものに特許(第6143809号)が設定されています。
後発品メーカーが先発品と同じ条件で薬を売り出すためには、この特許をクリアしなければなりません。そのため、沢井製薬、ニプロ、東和薬品といった後発品大手がタッグを組み、特許の無効を訴えていました。
2. 知財高裁の判決:後発品側に軍配
今回のニュースのポイントは、知財高裁が「この特許は無効である」という判断を改めて示したことです。
-
経緯: 2025年に特許庁が無効審決を下しましたが、先発メーカー側がこれを不服として訴訟を起こしていました。
-
今回の結果: 知財高裁も特許庁の判断を支持し、無効を維持しました。
専門家からは、「トラゼンタの承認内容と直結する特許であるため、この無効が確定すれば後発品参入への最大の壁が取り払われることになる」との分析が出ています。
3. トラゼンタを巡る巨額の市場
なぜこれほどまでに激しい法的争いが起きているのでしょうか。それはトラゼンタが持つ市場規模の大きさにあります。
-
売上規模: 2024年度の薬価ベースで約341億円。
-
特許切れのタイミング: 物質特許は2024年3月に満了。
-
後発品のターゲット: 2026年12月の薬価収載を目指す動きが活発化しています。
これだけのシェアを持つ薬剤の後発品となれば、メーカー各社にとって極めて重要な戦略製品となるのは間違いありません。
4. まだ「不透明」な部分も。今後の注目ポイント
今回の判決は後発品参入にとって大きな前進ですが、まだ「完全決着」とは言い切れません。
-
最高裁への上告はあるか?
先発メーカー側が最高裁に上告する可能性が残されています。 -
他にも存在する特許の存在
トラゼンタには他にも「特定の患者群に関する特許」など、複数の特許が網の目のように張り巡らされています。これらについても現在、無効審判や訴訟が続いています。
ジャヌビア後発品訴訟、サワイ側が特許侵害を認める
糖尿病患者さんに広く処方されている薬「ジャヌビア」。この薬の「安価な後発品(ジェネリック)」をいち早く出そうとしていた沢井製薬(サワイグループ)と、先発品を守りたいメルク(MSD)との間で争われていた裁判が、意外な形で幕を閉じました。
1. 何が争点だったのか?(水和物があるかないかの違い)
ジャヌビアの主成分は「シタグリプチン」という物質です。
-
先発品(MSD): 物質に水分子が含まれる「シタグリプチンリン酸塩水和物」として特許を取っています。
-
後発品(沢井): 特許を避けるため、水分子を含まない「無水物」として承認を得ました。
沢井側は「水がないタイプだから、先発品の特許には当たらない(特許回避)」という戦略で、他社に先駆けて発売を目指していました。
2. 裁判の結果:サワイ側の「全面認諾」
これに対し、メルク側は「無水物であっても、特許の効力は及ぶはずだ」と訴えを起こしていました。
約2年にわたる審理の結果、サワイ側はメルク側の主張をすべて受け入れました(認諾)。 つまり、「無水物でも特許侵害になります」ということを沢井が正式に認めた形です。
3. ジェネリック医薬品はいつ発売されるの?
「ジャヌビアのジェネリックはいつ安く手に入るの?」という点については、以下の通りです。
-
発売は延期: サワイ側が特許侵害を認めたため、少なくとも先発品の特許が切れるまでは発売されない見通しです。
-
損害賠償はなし: 幸い、サワイ側はまだこの薬を実際に発売(薬価収載)していなかったため、メルク側への賠償金などは発生しません。
4. サワイの今後の戦略は?
沢井製薬(サワイHD)は、これまで「他社が手を出さないような特許の隙間を突いて、一番乗りで後発品を出す」という攻めの知財戦略をとってきました。
今回の件は、その戦略が一部裏目に出た形ですが、同社は「今後の開発戦略や方針に変更はない」としています。今後も、特許の壁に挑戦する姿勢は変えないようです。
尚、同じDPP4阻害剤のトラゼンタに関しては、2026年度中にジェネリック医薬品の発売を狙っているGEメーカーと、開発元のベーリンガーインゲルハイムとの間で特許侵害についての論争が水面下で行われています。
糖尿病治療薬「トラゼンタ」のジェネリックはいつ出る?
2型糖尿病の治療でよく処方されるお薬「トラゼンタ(一般名:リナグリプチン)」。
1日1回飲むだけで済み、さらに腎臓が弱い人でも使いやすいという特徴から、国内でもトップクラスの売上を誇る人気のお薬です。
そんなトラゼンタですが、実は今、「ジェネリック医薬品(後発品)」をいつ発売できるかを巡って、ジェネリックメーカー各社と、開発元のメーカーの間で激しい火花が散っています。
1. 「2026年末」の発売を目指して、ジェネリック各社が動き出す!
通常、お薬の特許が切れると、安価なジェネリック医薬品が登場します。トラゼンタの場合、一番の大元となる特許(物質特許)がもうすぐ切れるため、2026年12月のジェネリック発売が大きなターゲットとなっています。
しかし、すんなり発売とはいきません。開発元の日本ベーリンガーインゲルハイム社は、大元の特許以外にも、
-
「1日1回5mg」という飲み方に関する特許
-
特定の病気を持つ人への使い方に関する特許
など、いくつもの「守りの特許」を持っています。これらが壁となり、ジェネリック各社は思うように準備が進められない状況にあるのです。
2. 「沢井・ニプロ」など大手4社が裁判で訴え
この高い壁を崩そうと、ジェネリック大手である沢井製薬、ニプロ、東和薬品、日本ジェネリックの4社が立ち上がりました。
彼らは「それらの特許は無効であるべきだ」と主張し、なんと20件近い無効審判(裁判のようなもの)を申し立てています。
「特許が有効ならジェネリックは出せない(または使い方が制限される)」
「無効になれば、予定通り安く提供できる」
という、まさに生き残りをかけた戦いです。
3.2026年2月9日の「判決」が大きな分かれ目に
特に注目されているのが、「1日1回5mg」という飲み方の特許です。
実は、一度は「この特許は無効」という判断が出たのですが、現在は知財高裁(知的財産高等裁判所)でさらに争われています。その最終的な判決が、来週の2月9日に出る予定です。
ここでどのような結論が出るかによって、2026年に無事にジェネリックが発売されるか、あるいは大幅に制限されるか、運命が決まると言っても過言ではありません。
トラゼンタとその配合剤(トラディアンス)は、年間で合わせて約700億円近くも売れている巨大な市場です。もしジェネリックが登場すれば、患者さんの窓口負担が減るだけでなく、国の医療費抑制にも大きく貢献します。
しかし、新薬メーカーにとっては心血を注いで開発した権利を守りたいという思いがあります。
ジャヌビア”が「シタグリプチンリン酸塩水和物」で、”ジェネリック”が「シタグリプチンリン酸塩」である点について
2023年10月27日追記
ジャヌビア錠を製造販売するMSDは沢井製薬とサワイグループHDのグループ会社「メディサ新薬」に対して、DPP-4阻害薬シタグリプチンの特許権を侵害したとして、特許侵害訴訟および仮処分申請を東京地裁に行いました。
MSD側は「ジャヌビアのすべての剤形のさまざまな側面をカバーする単数又は複数の特許が有効であると確信している」とコメントしています。
ジャヌビア錠/グラクティブ錠の一般名が「シタグリプチンリン酸塩水和物」であるのに対して、2023年12月に沢井から発売されるジェネリック医薬品は「シタグリプチンリン酸塩」であり、”水和物”がついていません。
2023年12月にGEを発売する見込みの沢井製薬側の主張としては「水和物」がついていない「シタグリプチンリン酸塩」には、特許はないため販売可能であるというのが主訴のようです。
このような経緯になった背景と、我々現場の対応について以下に記します。
ジャヌビア錠の一般名は「シタグリプチンリン酸塩水和物」であり、2009年10月に承認された医薬品です。2022年7月に特許期間が満了となるはずだったのですが、特許延長が認められ2025年2月~2026年3月ごろに特許が切れる予定となりました。
この特許延長に関してMSDは「シタグリプチンリン酸塩水和物」で特許延長を出願して、延長が認可されました。
「シタグリプチンリン酸塩」(水和物なし:無水物)に関しては、2022年7月に特許が満了したままではないか?と考えて、サワイHDは「シタグリプチンリン酸塩」(水和物なし:無水物)を承認申請したところ、厚生労働省により承認されたという経緯です。
このような流れから、大人気DPP4阻害薬であるジャヌビア錠/グラクティブ錠のジェネリック医薬品に関して、メディサ新薬株式会社(サワイHD)が1社だけで承認申請を取得したわけです。
水和物か無水物について、特許侵害となるか否かについては司法が判断するわけですから、我々医療現場の人間には対岸の話です。
現場第一の私としては以下の2点が気になりました。
・先発品が「○○水和物」で後発品が「○○(無水物)」という薬は薬価収載されている薬の中にあるのだろうか?(GEへ変更調剤可能か?)
・水和物か無水物かで薬効は変わらないのか?
という点です。
まず最初のギモンについて、厚生労働省の薬価基準収載品目リストを確認したところ、内服薬に1種類だけ該当する品目をみつけました。
先発品「スプリセル錠20mg/50mg(ダサチニブ水和物)」
後発品「ダサチニブ」
です。
実際に添付文書の一番下に記載されている構造式を確認してみました。
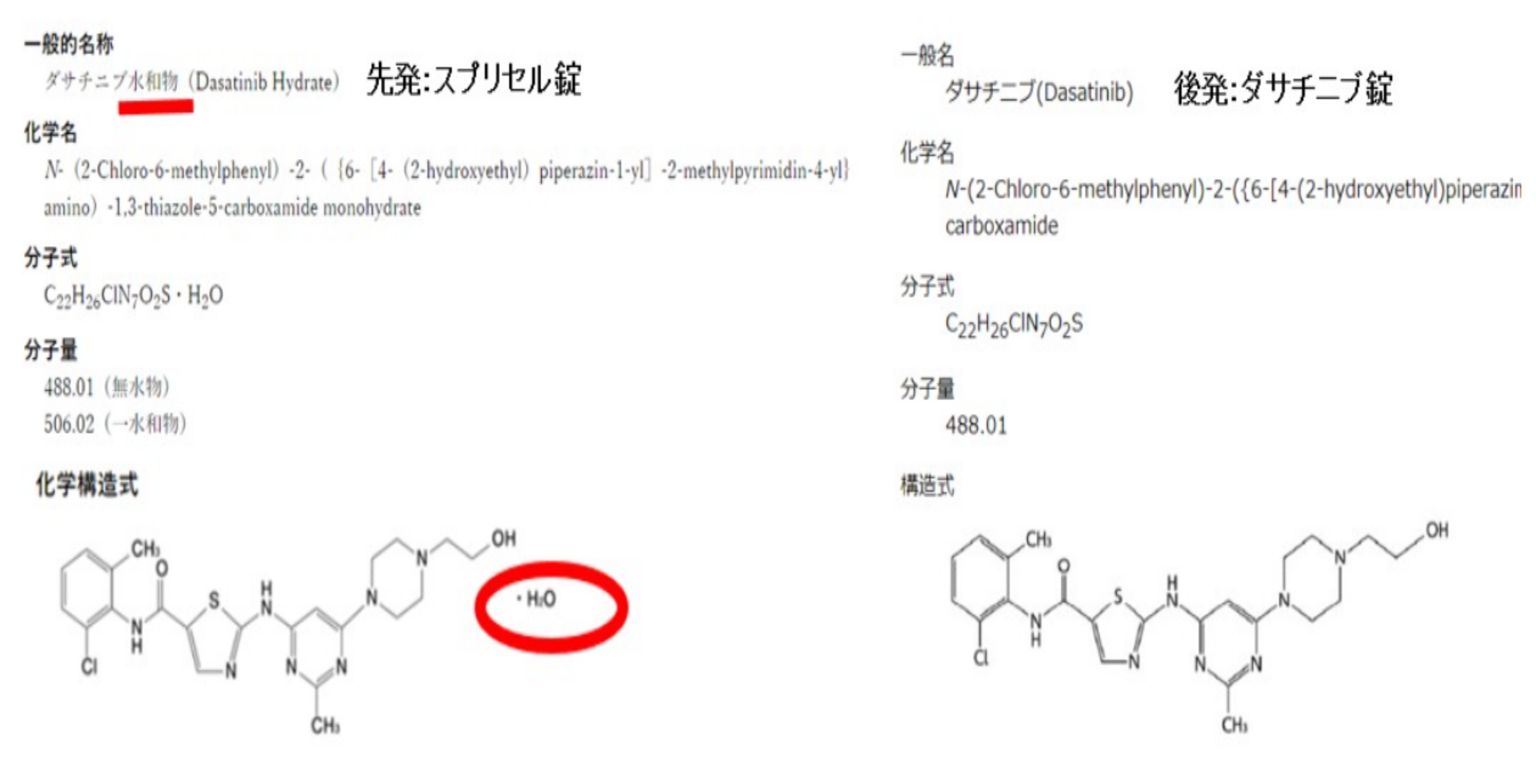
dasatinib
左側が先発品「スプリセル錠」の構造式で、右側がジェネリック医薬品の構造式です。
赤丸で記したように、先発品にはH2Oが付加されていますが、後発品にはついていません。
つまり、水和物がついていても、ついていなくても(無水和物)、ジェネリック医薬品として認可されて医療現場で使用されていることが見て取れます。
上記の例は1例しか見つけることができなかったのですが、逆パターンも見つけることができました。
帯状疱疹で使用するバルトレックス錠についてんなのですが、バルトレックス錠の一般名は「バラシクロビル塩酸塩」であるのに対し、バラシクロビル「トーワ」の一般名は「バラシクロビル塩酸塩水和物」と記載され、実際に添付文書の構造式を見てみると、水和物が付加していることがわかります。
上記の結果より、先発品が〇〇水和物、後発品が無水和物であってもGE変更が可能であることが推測されます。
次に、水和物・無水和物でも効能効果が変わりないことを確認します。
水和物と無水和物とでは、温度、湿度、圧力、賦形などに対する安定性が異なります。一般的に水和物は無水和物よりも溶解速度が大きいことが知られています。
そのため、シタグリプチンリン酸塩「サワイ」の添付文書が公開された際には、CmaxやTmax、AUCの値がどの程度標準品と差があるかを確認する必要があります。
とはいえですね、例えば飲んですぐに効き目が期待される「即効性の薬」であれば水和物か無水和物かというのは非常に重要なポイントの一つとなるのですが、ジャヌビアは半減期が12時間の薬であり、即効性を期待する薬ではなく、定常状態を維持し続けることで血糖値を低く保つ薬です。
つまり、ジャヌビア(シタグリプチンリン酸塩水和物)に関しては、溶出速度はさほど大きな問題ではなく、先発と後発で同等のAUCが確認できればいいのではないかと私は個人的に考えます。
最期に、雑談ですが、医薬品の一般名として
「他の製剤との混同を招かないと判断される場合にあっては、塩、エステル及び水和物等に関する記載を省略することが可能である」
というルールがあります。
例えば「オノンカプセル」の一般名は、添付文書の「禁忌」の上部分に「プランルカスト水和物」と記されています。
ジェネリック医薬品の「プランルカスト「サワイ」の一般名は、添付文書の「禁忌」の上部分には「プランルカストカプセル」と記されています。この場合、プランルカスト「サワイ」の一般名に記されている「プランルカストカプセル」について、水和物が省略されているのか、はたまは「無水和物?」なのかの区別はできません。
そこで、「プランルカスト「サワイ」の添付文書を一番下まで見てみます。
すると「有効成分に関する理化学的知見」の部分に
一般名:プランルカスト水和物
と記載されており、ジェネリック医薬品の「プランルカスト「サワイ」の一般名が先発の「オノン」と同じであることが確認されます。
そのため、先発が○○水和物、後発が「無水和物」という医薬品の例は、非常に探しにくく、かつ非常に稀であると私は感じています。
余談でした。