多発性硬化症と視神経脊髄炎の症状から新薬の仕組みまで徹底解説
1. 中枢神経を守る「絶縁体」が壊れる仕組み
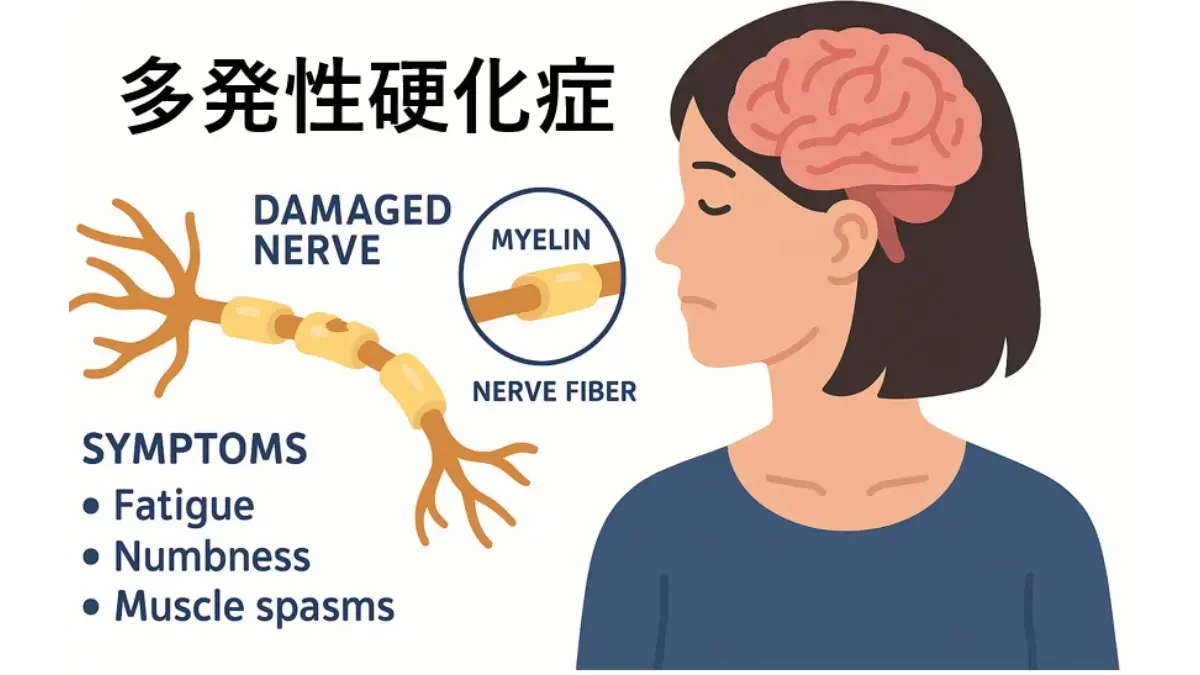
私たちの脳や脊髄(中枢神経)は、電気信号を使って情報を伝達しています。この信号が通る神経線維を、電気コードのビニール被覆のように覆っているのが「髄鞘(ずいしょう)」です。
多発性硬化症(MS)や視神経脊髄炎スペクトラム障害(NMOSD)は、本来自分を守るはずの免疫システムが、誤ってこの「髄鞘」を攻撃してしまう自己免疫疾患です。これを「脱髄(だつずい)」と呼びます。被覆が剥がれた電気コードがショートするように、情報の伝達がうまくいかなくなり、さまざまな症状が引き起こされます。
多発性硬化症(MS)の特徴
MSは、中枢神経のいたるところに「多発」して病変ができ、時間の経過とともに症状が良くなったり悪くなったり(再発と寛解)を繰り返すのが特徴です。日本では人口10万人あたり約14.3人と、以前の調査(5.2人)から2倍以上に増えています。
視神経脊髄炎(NMOSD)の特徴
NMOSDは、主に視神経と脊髄を狙い撃ちにする非常に激しい炎症です。多くの場合、「アクアポリン4(AQP4)」という細胞の水の通り道を攻撃する異常な抗体(AQP4抗体)が原因であることが判明しています。
2. 見逃してはいけない初期症状と自覚症状
病変ができる場所によって症状は千差万別ですが、多くの患者さんが最初に経験する症状には共通点があります。
視覚の異常(視神経炎)
-
片方の目が急に見えにくくなる。
-
目を動かすと奥の方が痛む。
-
色が鮮やかに見えなくなる。
感覚・運動の異常(脊髄炎など)
-
手足がしびれる、ジンジンする。
-
お風呂に入ったときに、お湯の熱さを感じにくい。
-
足がもつれる、力が入らない。
-
「レルミット徴候」:首を前に曲げると、背中から足にかけて電気が走るような衝撃を感じる。
-
「ウートフ現象」:体温が上がると(入浴や運動後)、一時的に症状が悪化する。
その他の症状
-
強い疲労感(倦怠感)。
-
排尿障害(トイレが近い、出にくい)。
3. 多発性硬化症(MS)の治療薬:最新の薬理作用とエビデンス
多発性硬化症の治療目標は、再発を抑えるだけでなく、将来的な身体障害の進行を最小限にすることです。現在、日本で認可されている主要な8種類の薬剤について詳しく見ていきましょう。
① インターフェロンベータ(ベタフェロン、アボネックス)
開発背景: 1990年代に最初に登場した多発性硬化症の基本薬です。
薬理作用: 細胞表面にある「IFNAR受容体」に結合します。これにより、炎症を引き起こす物質(サイトカイン)の産生を抑え、逆に炎症を鎮める物質を増やすことで、免疫のバランスを整えます。
効能効果: 21年間にわたる長期の追跡調査では、プラセボ(偽薬)を投与された群と比較して、死亡リスクを46.8%減少させたという驚くべきデータがあります。
持続時間: ベタフェロンは隔日、アボネックスは週1回の投与で効果を維持します。
② フィンゴリモド(イムセラ、ジレニア)
薬理作用: リンパ球の表面にある「S1P受容体」に作用します。通常、リンパ球はS1Pというリガンド(結合物質)の濃度勾配を頼りにリンパ節から外へ出ますが、この薬が受容体に結合して細胞内に取り込ませてしまうことで、リンパ球をリンパ節内に閉じ込めます。脳や脊髄へ攻撃部隊(リンパ球)を行かせない「関所」のような役割をします。
効能効果: 国際共同試験(FREEDOMS試験)において、年間再発率をプラセボと比較して55%低下させました。
発動・持続時間: 投与開始から数時間でリンパ球減少が始まり、毎日服用することで安定した効果が持続します。
③ シポニモド(メーゼント)
開発背景: 再発を繰り返した後に徐々に障害が進む「二次性進行型MS(SPMS)」のために開発されました。
薬理作用: フィンゴリモドをより改良し、S1P受容体のタイプ1と5に「選択的」に作用します。これにより、副作用を抑えつつ、中枢神経内の炎症抑制と神経保護効果の両立を狙っています。
効能効果: EXPAND試験において、3カ月間持続する身体障害の進行リスクを21%低下させました。
④ フマル酸ジメチル(テクフィデラ)
薬理作用: 細胞内の「Nrf2経路」という酸化ストレスに対する防御スイッチをオンにします。これにより、神経細胞を炎症によるダメージから守りつつ、免疫細胞の暴走を抑えます。
効能効果: 2年間の試験で、再発患者の割合をプラセボに対し49〜50%減少させました。
⑤ ナタリズマブ(タイサブリ)
薬理作用: リンパ球の表面にある「α4インテグリン」という接着分子に結合するヒト化モノクローナル抗体です。脳の血管の壁にある「VCAM-1」というリガンドとの結合をブロックし、リンパ球が血管の壁を通り抜けて脳内へ侵入するのを完全に阻止します。
効能効果: 極めて強力で、MRI検査での新規病変を83〜92%減少させます。
持続時間: 4週間に1回の点滴(最近では6週間に1回の延長投与も行われます)で効果が持続します。
⑥ オファツムマブ(ケシンプタ)
開発背景: 病院での点滴ではなく、自宅で「自己注射」ができる利便性を求めて開発された最新の抗体製剤です。
薬理作用: B細胞という免疫細胞の表面にある「CD20受容体」に強く結合し、補体や他の免疫細胞の力を借りてB細胞を直接破壊・除去(枯渇)させます。
効能効果: teriflunomide(既存薬)との比較試験において、年間再発率を50〜60%もさらに減少させました。
発動・持続時間: 投与から迅速にB細胞を消失させ、月1回の注射で維持します。
4. 視神経脊髄炎(NMOSD)の治療薬:補体とサイトカインの阻止
NMOSDの治療は、MSとは全く異なるメカニズムで行われます。特に「補体」と「IL-6」という物質を抑えることが重要です。
① エクリズマブ(ソリリス)
薬理作用: 免疫反応の最終段階で細胞を破壊する「補体C5」というタンパク質をブロックします。AQP4抗体が細胞に結合しても、この薬が補体の活性化を止めるため、視神経や脊髄の細胞が破壊されずに済みます。
効能効果: PREVENT試験において、プラセボ群と比較して再発リスクを94%(ハザード比0.06)という圧倒的な数値で減少させました。
② サトラリズマブ(エンスプリング)
薬理作用: 炎症の司令塔である「IL-6受容体」に結合し、炎症のシグナル伝達を遮断します。
効能効果: AQP4抗体陽性例において、再発リスクを74〜79%減少させました。4週間に1回の皮下注射で治療可能です。
③ イネビリズマブ(ユプリズナ)
薬理作用: 「CD19受容体」を持つB細胞(抗体を作る元になる細胞)を幅広く除去します。
効能効果: AQP4抗体陽性例で再発リスクを77.3%減少させました。半年間に1回の点滴で済むため、生活の質(QOL)が高いのが特徴です。
5. 治療薬を使用する際の副作用について
どんなに優れた薬にも副作用のリスクは存在します。治療を継続するためには、これらを正しく理解し、医師と共有することが不可欠です。
-
注射部位反応: ケシンプタやコパキソンなどで見られる、皮膚の赤みや痛みです。
-
インフルエンザ様症状: インターフェロン製剤の投与後に発熱やだるさが出ることがありますが、多くは徐々に慣れていきます。
-
進行性多巣性白質脳症(PML): タイサブリやジレニアなどで稀に起こる、ウイルスによる深刻な脳感染症です。JCV抗体検査を定期的に行うことでリスクを管理します。
-
感染症のリスク: 抗体製剤(ケシンプタ、ユプリズナなど)は免疫を抑えるため、風邪や帯状疱疹などにかかりやすくなることがあります。
-
髄膜炎菌感染症: ソリリス使用時には特に注意が必要で、あらかじめワクチンの接種が義務付けられています。
-
潮紅・胃腸障害: テクフィデラで見られる顔のほてりや胃痛です。食事と一緒に服用することで軽減できます。

6. まとめ
「早期診断を行い、患者さん一人ひとりの予後不良因子(進行しやすいサイン)を見極め、適切な強度の薬剤を速やかに導入すること」です。
かつては「第一選択薬(マイルドな薬)」から始め、効果がなければ強い薬に変える「エスカレーション療法」が主流でした。しかし現在では、最初から強力な「高力価薬」を使用することで、長期的な身体障害の進行を大幅に抑えられるというエビデンスが確立されています。
治療薬の選択肢が増えた今、医師と患者さんが「どんな生活を送りたいか」という価値観を共有し、共に治療方針を決める(シェアード・ディシジョン・メイキング)ことが、最も重要な治療の第一歩となります。しびれや視力低下といった「サイン」を感じたら、一人で悩まずに専門医(脳神経内科)を受診してください。適切な治療により、多くの患者さんが自分らしい生活を送り続けることが可能な時代になっています。